长生生物疫苗造假事件最新消息 已收到罚单被罚没344万元

7月19日晚,长生生物发布公告,称已于7月18日收到《吉林省食品药品监督管理局行政处罚决定书》。
《决定书》显示,长生生物生产的“吸附无细胞百白破联合疫苗”,经中国食品药品检定研究院检验,检验结果【效价测定】项不符合规定。公司行为违反了《中华人民共和国药品管理法》第四十九条第一款“禁止生产、销售劣药。”之规定。于2017年10月27日予以立案调查。
依据《中华人民共和国药品管理法》第七十四条、《中华人民共和国药品管理法实施条例》第七十三条相关规定,吉利食药监管局决定没收长生生物库存的“吸附无细胞百白破联合疫苗”186 支; 没收违法所得85.9万元;处违法生产药品货值金额三倍罚款258万元。合计罚款344万元。
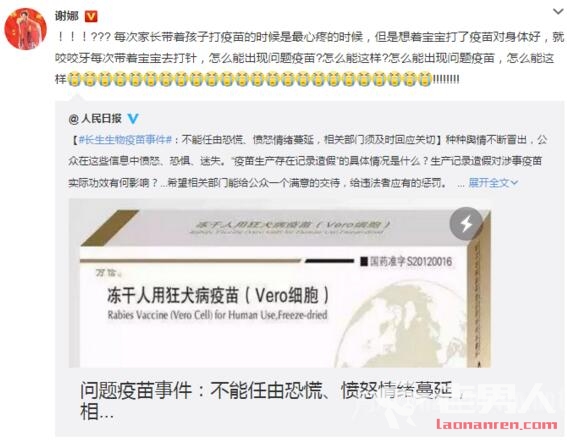
7月15日下午,国家药监局发布公告,称长春长生(长生生物子公司)冻干人用狂犬疫苗生产存在记录造假等违法违规行为,已经进驻调查该企业,并收回药品GMP证书,责令停止生产。消息一出,举国震惊。
同一天,长生生物向各省推广团队发布紧急通知:立即停止使用公司的狂犬疫苗;立即就地封存我公司狂犬疫苗;公司立即启动召回程序。
7月17日,长生生物在官网道歉,称此次飞行检查所有涉事疫苗尚未出厂销售,全部产品已经得到有效控制。这一天,长生生物收到了深交所的关注函,要求公司说明冻干人用狂犬病疫苗的具体产量、销量和销售金额、此次GMP证书被收回的具体原因及事实、相关产品流向市场的风险以及对2018年生产经营产生的影响等。
7月18日,长生生物发布2018年上半年业绩修正报告,将净利润区间由3.44亿至4.23亿元下调至2.11亿至3.17亿元。这一天,国家卫健委回应此次事件称,密切关注事态发展。
受此影响,长生生物已经连续4天“一字板”跌停。截至7月19日收盘,报收16.11元,4天市值蒸发超82亿。

以下为文字:
在国家药品专项抽验中,你公司生产的“吸附无细胞百白破联合疫苗”(批号:201605014-01),经中国食品药品检定研究院检验,检验结果【效价测定】项不符合规定。你公司生产的上述药品符合《中华人民共和国药品管理法》第四十九条第三款第六项“其他不符合药品标准规定的”规定的情形,应按劣药论处。
你公司的行为违反了《中华人民共和国药品管理法》第四十九条第一款“禁止生产、销售劣药。”的规定,于2017年10月27日予以立案调查。
经查明,该批药品生产数量共253338支,由吉林省药品检验所抽样552支, 销售到山东省疾病预防控制中心252600支,现库存186支,销售价格是3.40元/ 支,该批药品的违法所得共858840.00元,货值金额共861349.20元。
处罚依据和种类:
你公司的上述行为已违反了《中华人民共和国药品管理法》第四十九条第一款“禁止生产、销售劣药。”之规定。依据《中华人民共和国药品管理法》第七十四条:“生产、销售劣药的,没收违法生产、销售的药品和违法所得,并处违 法生产、销售药品货值金额一倍以上三倍以下的罚款;情节严重的,责令停产、停业整顿或者撤销药品批准证明文件、吊销《药品生产许可证》、《药品经营许可证》或者《医疗机构制剂许可证》;构成犯罪的,依法追究刑事责任。”的规定、《中华人民共和国药品管理法实施条例》第七十三条:“违反《药品管理法》 和本条例的规定,有下列行为之一的,由药品监督管理部门在《药品管理法》和本条例规定的处罚幅度内从重处罚:(二)生产、销售以孕产妇、婴幼儿及儿童为主要使用对象的假药、劣药的;(三)生产、销售的生物制品、血液制品属于假药、劣药的;”的规定,参照《吉林省食品药品监督管理系统行政处罚裁量规则》第十一条:“当事人有下列情形之一的,应当依法予以从重处罚:(九)其他法律、行政法规明确规定的从重处罚的情形。”
本局决定对你公司给予以下行政处罚:
1、没收库存的“吸附无细胞百白破联合疫苗”(批号:201605014-01)186 支;
2、没收违法所得858840.00元。
3、处违法生产药品货值金额三倍罚款2584047.60元。罚没款总计3442887.60 元(叁佰肆拾肆万贰仟捌佰捌拾柒元陆角整)。