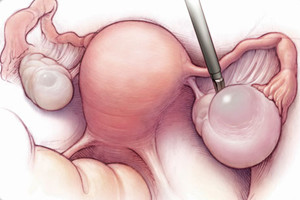
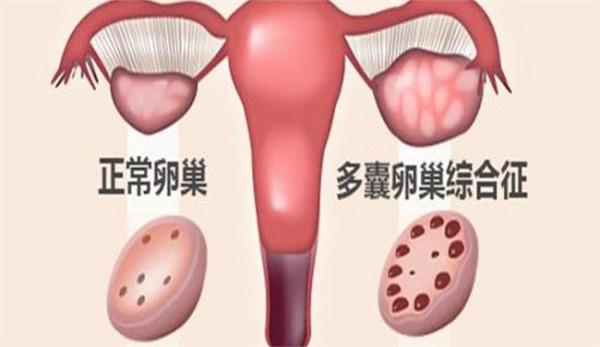
得了多囊卵巢怎么办呢 5大治疗方法你了解吗
病因
PCOS的病因尚不清楚,涉及的病理机制非常复杂。一般认为与下丘脑-垂体-卵巢轴功能失常、肾上腺功能紊乱、遗传、代谢等因素有关。
1.遗传学因素
PCOS是一种常染色体显性遗传,或X—连锁(伴性)遗传,或基因突变所引起的疾病。多数患者染色体核型46,XX,部分患者呈染色体畸变或嵌合型如46,XX/45,XO/46,XX/46,XXq和46,XXq。
2.肾上腺初现假说
PCOS起源于青春期前肾上腺疾病,即当受到强烈应激刺激时网状带分泌过多雄激素,并在性腺外转化为雌酮,反馈性地引起HP轴GnRH-GnH释放节律紊乱,LH/FSH比值升高,继发引起卵巢雄激素生成增多,即肾上腺和卵巢共同分泌较多雄激素致高雄激素血症。高雄激素血症在卵巢内引起被膜纤维化增厚、抑制卵泡发育,造成卵巢囊性增大和慢性无排卵。
中医认为本病主要是因肾虚、痰湿、气滞血瘀、肝经湿热等导致的肾-天癸-冲任-胞宫轴功能失调,致使月经停闭、不孕等。
检查
1.激素测定
睾酮增高和(或)血清LH/FSH≥2.5~3:约75%患者LH升高,血LH与FSH比值与浓度均异常。
2.影像学检查
(1)盆腔b超卵巢增大,每平面至少有10个以上2~6mm直径的卵泡,主要分布在卵巢皮质的周边,少数散在于间质中,间质增多。
(2)气腹摄片双侧卵巢增大2~3倍,若雄激素的主要来源为肾上腺,则卵巢相对较小。
(3)腹腔镜(或手术时)见卵巢形态饱满、表面苍白平滑、包膜厚、有时可见其下有毛细血管网。因外表颜色呈珍珠样,俗称牡蛎卵巢,表面可见多个囊状卵泡。
(4)经阴道超声经阴道超声100%可探测多囊卵巢,而经腹部有30%的病人漏诊。对于未婚肥胖的患者可应用肛门超声来检测,可见一侧或两侧卵巢各有10个以上直径为2~9mm无回声区,围绕卵巢边缘,呈车轮状排列,称为项链征。连续监测未见优势卵泡发育及排卵迹象。部分PCOS患者的超声相可正常。
(5)其他腹部肥胖者应测空腹血糖及口服葡萄糖耐量试验,还应测空腹胰岛素及葡萄糖负荷后血清胰岛素。肥胖型患者可有甘油三酯增高。
3.剖腹探查
拟诊卵巢肿瘤或欲行卵巢楔切时施行。
4.其他检查
(1)阴道脱落细胞成熟指数是初步了解体内性激素状况的简易方法。睾酮过多的涂片往往出现3层细胞同时存在的片型,明显增高时3层细胞数几乎相等,但必须与炎症相区别。雌激素水平可以从表层细胞百分比来估计,但不能反映血液中激素的含量。
(2)基础体温测定判断有无排卵,排卵者呈双相型,无排卵者一般为单相型。
诊断
1.临床诊断
初潮后多年月经仍不规则、月经稀少和(或)闭经,同时伴肥胖与多毛、婚后不孕等,应疑诊PCOS。典型病例具有上述各种症状及体征,即月经失调、多毛、痤疮、肥胖、不孕等。非典型病例可表现为:①单纯性闭经不伴有肥胖、多毛及卵巢肿大,排除其他各种疾病,而孕酮试验阳性者,仍应考虑为PCOS。②排卵型功能失调性出血。③月经异常合并多毛。④月经异常伴男性化症状,无明显肥胖。⑤功能失调性子宫出血伴不育。
对于不典型病例需详细询问有关病史,如起病年龄、生长发育情况,起病经过,用药史,家族史,个人生活习惯,既往有无全身性疾病。结合辅助检查,排除其他疾病,并经b超等检查明确诊断。
2.诊断标准
由于本病的异质性,诊断标准尚未统一,多数学者根据青春期发病、月经和排卵异常、多毛、血LH和(或)LH/FSH比值升高,结合雄激素水平过高,超声检查有多囊卵巢征象,排除其他类似疾病后,可确定本症的诊断。
治疗
1.肥胖与胰岛素抵抗
增加运动以减轻体重,纠正由肥胖而加剧的内分泌代谢紊乱,减轻胰岛素抵抗和高胰岛素血症,使IGF-1降低,IGfBP-1增加,同时SHBG增多使游离雄激素水平下降。减轻体重可使部分肥胖型PCOS者恢复排卵,并可预防2型糖尿病及心血管疾病的发生。二甲双胍治疗,伴或不伴有糖尿病者均可使用,能有效地降低体重,改善胰岛素敏感性,降低胰岛素水平,使毛发减少甚至可恢复月经(25%)与排卵。由于肥胖和胰岛素抵抗是PCOS的主要病因,故凡可减轻体重与增加胰岛素敏感性的药物均可治疗本综合征。
2.药物诱导排卵
(1)氯米芬是PCOS的首选药物,排卵率为60%~80%,妊娠率30%~50%。氯米芬与下丘脑-垂体水平的内源性雌激素竞争受体,抑制雌激素负反馈,增加GnRH分泌的脉冲频率,从而调整LH与FSH的分泌比例。氯米芬也直接促使卵巢合成和分泌雌激素。服用本药后,卵巢因过度刺激而增大(13.6%),血管舒张而有阵热感(10.4%)、腹部不适(5.5%)、视力模糊(1.5%)或有皮疹和轻度脱发等副作用。
治疗期间需记录月经周期的基础体温,监视排卵,或测定血清孕酮、雌二醇以证实有无排卵,指导下次疗程剂量的调整。若经氯米芬治疗6~12个月后仍无排卵或受孕者,可给予氯米芬加HCG或糖皮质激素、溴隐亭治疗或用HMG、FSH、GnRH等治疗。
(2)氯米芬与绒促性素(HCG)合用停用氯米芬后第7天加用绒促性素(HCG)。
(3)糖皮质激素与氯米芬合用肾上腺皮质激素的作用是基于它可抑制来自卵巢或肾上腺分泌的过多雄激素。通常选用地塞米松或泼尼松。2个月内有效率35.7%,闭经无排卵者的卵巢功能得到一定恢复。用氯米芬诱发排卵无效时,可在治疗周期中同时加服地塞米松。
(4)尿促性素(HMG)主要用于内源性垂体促性腺激素与雌激素分泌减少的患者,尿促性素(HMG)是从绝经期妇女尿中纯化的提取物,内含FSH与LH,两者比例为1∶1,每安瓿含FSH和LH各75U。尿促性素(HMG)被视为治疗无排卵不孕的备选诱发排卵药物,因其副作用较多,诱发卵巢过度刺激综合征(OHSS)的危险性较大。绒促性素(HCG)的治疗剂量应因人及治疗周期而异,并备有严密的卵泡成熟监测措施,防止发生卵巢过度刺激综合征(OHSS)。
(5)促性腺激素释放激素(GnRH)GnRH可促进垂体的FSH和LH释放,但长期应用使垂体细胞的GnRH受体不敏感,导致促性腺激素减少,从而减少卵巢性激素的合成。其作用可逆,开始对垂体的FSH、LH和卵巢的性激素起兴奋作用,14天后下降至正常水平,28天达去势水平。但由于GnRH-A价值昂贵,用量大,临床应用受到限制。
(6)FSHFSH有纯化的和重组的人FSH(rhFSH)2种。FSH是多囊卵巢较理想的治疗制剂,但价格昂贵。并可能引起OHSS。应用过程中,必须严密监测卵巢变化。FSH也可与GnRH-A联合应用,以提高排卵成功率。
(7)溴隐亭适用于伴有高PRL的ICOS患者餐后服用。
3.双侧卵巢楔形切除
适用于血睾酮升高、双侧卵巢增大而DHEA、PRL正常(提示主要病因在卵巢)者,切除部分卵巢,去除卵巢产生过多的雄激素,可纠正下丘脑-垂体-卵巢轴的调节紊乱,但切除的部位和切除的组织量与疗效有关,有效率不等。妊娠率为50%~60%。术后复发率高,如并发盆腔粘连,则不利于妊娠。腹腔镜下卵巢烧灼术或切除术亦可收到一定效果。
4.多毛症治疗
可定期剪去或涂以“脱发剂”,切忌拔除,以防刺激毛囊过度生长,亦可作电蚀治疗或应用抑制雄激素药物治疗。
(1)口服避孕药以雌激素为主的雌、孕激素复合片较理想,可抑制LH分泌,降低血睾酮、雄烯二酮和DHEAS,增加性激素结合球蛋白浓度。
(2)孕激素有弱的抗雄激素和轻度抑制促性腺激素分泌的作用,可降低睾酮和17-酮类固醇的水平。以甲羟孕酮(安宫黄体酮)较常用。一般口服。此外,醋酸酯环丙孕酮(CPA)属高效孕酮,有较强抗雄激素作用。常与炔雌酮同服。
(3)GnRH-A在月经周期的第1~5天开始使用,现已有经皮吸入、皮下和肌内注射等多种制剂可供选用。同时加服炔雌酮可避免用药后雌激素所致的不良反应。
(4)地塞米松适用于肾上腺来源的高雄激素血症,每晚口服。
(5)螺内酯通过阻止睾酮与毛囊的受体结合,也可通过抑制17α-化酶而干扰卵巢雄激素的合成。可使患者的毛发生长减少,毛发变细。高雄激素血症伴无排卵的月经失调者可于月经的第5~21天使用,可使部分患者月经周期及排卵恢复。
5.人工月经周期
对于无多毛的患者而又无生育要求者,可给予孕激素行人工周期治疗,以避免子宫内膜的过度增生和癌变。